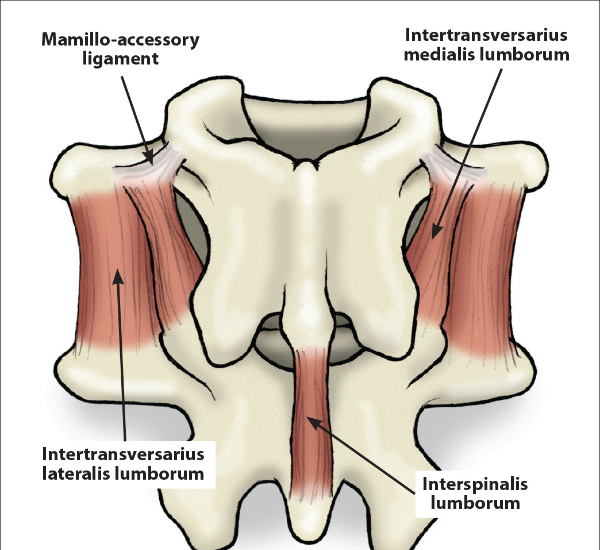
Отраженная боль
Отраженная боль - это боль, воспринимаемая совершенно в другом месте, а не в месте возникновения болезненного стимула или источника боли. [1]
Это результат сети взаимосвязанных сенсорных нервов, которые снабжают множество различных тканей. Когда есть повреждение в одном месте в сети, возможно, что когда сигнал интерпретируется в головном мозге, сигналы воспринимаются окружающей нервной тканью. [2]
🟣 Клинически значимая анатомия отраженной боли
Несколько нейроанатомических и физиологических теорий утверждают, что ноцицептивные нейроны дорсального рога и ствола головного мозга получают конвергентные входные сигналы от различных тканей.
🟪 Следовательно, более высокорасположенные центры не могут правильно определить фактический источник входного сигнала.
Недавние теории предложили модели, в которых пластичность нейронов спинного рога и ствола мозга играет центральную роль в возникновении отраженной боли. В течение последнего десятилетия была предпринята систематическая попытка нанести на карту мозга отраженные участки скелетно-мышечной боли. [1]
Нервные волокна более высоких сенсорных входов, таких как кожа, и нервные волокна более низких сенсорных входов, таких как желудок, сходятся на одном уровне спинного мозга. Это может привести к путанице сигналов в отношении того, откуда исходит ощущение или боль, так что стимул нижних сенсорных входов к мозгу можно интерпретировать как исходящий из более высоких областей, в результате чего ощущение боли располагается вдоль связанного дерматома того же позвоночного сегмента. [3]
Ярким примером этого явления является боль при ишемии сердца; боль ощущается в шее, левом плече и спускается вниз по левой руке. Отраженная боль возникает из-за того, что несколько первичных сенсорных нейронов сходятся в одном восходящем тракте. Когда болезненные стимулы возникают в висцеральных рецепторах, мозг не может отличить висцеральные сигналы от более общих сигналов, исходящих от соматических рецепторов. Это приводит к тому, что боль интерпретируется как исходящая из соматических областей, а не из внутренних органов. [4]
Имман и Сондерс предположили, что отраженная боль следовала за распределением склеротомов (мышцы, фасции и кости) чаще, чем за классическими дерматомами. [1] Сенсорными проявлениями клинической и экспериментальной мышечной боли являются диффузная ноющая боль в мышцах, боль, относящаяся к отдаленным соматическим структурам, и изменения поверхностной и глубокой чувствительности тканей в болезненных областях. [1]
Периферический вход от отраженной области боли задействован, но не является необходимой причиной возникновения отраженной боли.
Гипотетически конвергенция ноцицептивных афферентов на нейронах дорсального рога может опосредовать отраженную боль. [1]
Нейрофизиологические теории
Было предложено несколько нейрофизиологических теорий отраженной боли [1] :
• Теория конвергенции-проекции.
Это наиболее приемлемое объяснение, при котором боль вызвана конвергенцией афферентной информации висцеральных органов и органов соматического происхождения в одном и том же сегменте. Это вызывает гиперреактивность нейронов дорсального рога, которая интерпретируется как происходящая из одного и того же дерматома.
• Теория облегчения конвергенции
• Теория
аксон -рефлекса
• Теория
сверхвысокой возбудимости
• Теория таламической конвергенции
Эпидемиология и этиология
Наиболее частые причины отраженной боли - боль, исходящая от сегмента позвоночника, крестцово-подвздошного сустава, внутренние органы, опухоли, инфекции или связанные с ними проявления. [5] [6]
Также следует отметить, что боль всегда связана с нервом именно этой области. Например, когда задействован девятый черепной нерв (языкоглоточный нерв), боль ощущается глубоко в ухе. Это контрастирует с болью, расположенной выше, когда поражен тройничный нерв. [6]
Характеристики и клиническая картина [1]
Область отраженной боли связана с интенсивностью и продолжительностью боли.
Временное суммирование - мощный механизм возникновения отраженной мышечной боли.
Центральная гипервозбудимость важна для степени выраженности отраженной боли.
Пациенты с хроническими скелетно-мышечными болями отмечают увеличение области отраженной боли при экспериментальных стимулах.
Проксимальное распространение отраженной мышечной боли наблюдается у пациентов с хронической скелетно-мышечной болью, которая очень редко встречается у здоровых людей.
Соматосенсорные изменения, зависящие от модальности, происходят в указанных областях, что подчеркивает важность использования протокола мультимодального сенсорного теста во время осмотра пациента.
Диагностические процедуры
Клинические исследования отраженной боли ограничены предвзятостью из-за когнитивных, эмоциональных и социальных аспектов.
Боль - это многомерное и в высшей степени индивидуализированное восприятие, которое очень трудно количественно оценить и подтвердить в клинических условиях. При экспериментальной боли исследователи имеют возможность контролировать интенсивность стимула, его продолжительность, а также его модальность. [1]
С экспериментальной болью мы также можем оценить психологический вызванный ответ либо качество боли (используя, например, опросник Макгилла по боли), либо количество боли (используя, например, визуальные аналоговые оценки). [1]
Эндогенные методы не подходят для провокации отраженной боли, потому что они характеризуются высокой скоростью ответа и не очень подходят для изучения общих состояний боли. Но у них есть и недостаток, потому что они задействуют несколько или все группы мышц. Поэтому лучше использовать экзогенные модели провокации. [1]
Наиболее используемой экзогенной моделью является внутримышечная инфузия гипертонического раствора. После инфузии отраженная боль будет ощущаться в структурах на расстоянии от места инфузии. [1] Там она появится с задержкой примерно на 20 секунд по сравнению с местной болью [7] . Пациент будет ощущать эту боль как рассеянную и неприятную. [8]
Также другие альгогенные вещества, такие как брадикинин, серотонин, капсаицин и вещество P, могут быть использованы для провокации отраженной боли. [9] [10] [1] [2] [3]
Другой способ вызвать отраженную боль - использовать мышечную электростимуляцию. Требуется значительно более высокая интенсивность стимула, чтобы вызвать отраженную боль по сравнению с местной болью, и была обнаружена значительная положительная корреляция между интенсивностью стимула и оценками интенсивности местной боли и отраженной боли. [1] [4]
Результаты показывают нам, что существует значительная корреляция между размером местной боли и отраженных областей боли и оценками местного ощущения боли и оценками интенсивности отраженного ощущения боли. [1] [4]
Также усиление ноцицептивного воздействия, которое будет поступать в спинной рог или нейроны ствола мозга, что вызывает расширение рецептивных полей, может быть ответственным за расширение упомянутых областей, которые обнаруживаются во время усиленной внутримышечной стимуляции. [4]
Осмотр невролога
Было предложено несколько объяснений относительно расходящихся результатов, полученных при анестезии области отраженной боли [4] [1] :
Различия в количестве анестезируемых структур (кожа, подкожная ткань, фасция, мышцы, сухожилия, связки и кости). Это наиболее важный критерий, поскольку отраженные области боли и, особенно, отраженная висцеральная боль, обычно находятся в глубоких тканях, в которых полная анестезия указанной области боли затруднена. [1] [4]
Продолжительность и уровень местной боли. [1] [4]
Место локальной боли (кожа, внутренние органы и глубокие структуры). [1] [4]
Наблюдаются ли сенсорные изменения (гиперчувствительность) в указанном месте боли. [1] [4]
Несколько исследований показали, что площадь отраженной боли коррелирует с интенсивностью и продолжительностью мышечной боли, что соответствует наблюдениям за вторичной кожной гипералгезией. [6] [5]
Наиболее эффективным лечением хронической скелетно-мышечной боли является использование антагонистов NMDA-рецепторов (кетамина), это дает лучшие результаты, чем обычное лечение морфином. [1] [5] .
Также нанесение эвтектической смеси местных анестетиков на кожу чуть выше указанной области боли снизило указанную интенсивность боли на 22,7%. [6] Аналогичный результат был обнаружен после того, как этилхлорид распыляли на область боли, вызванную физиологическим раствором. [7]
Есть два метода блокирования всех афферентов из указанной области боли:
Дифференциальная блокада нервов с между местом стимуляции и соответствующей дистальной зоной.
Внутривенная регионарная анальгезия
Тем самым указанная интенсивность боли снизилась на 40,2%.
Другие способы лечения боли: [9]
Иглоукалывание [9]
Техники мануальной и остеопатической медицины [9]
Инъекции в триггерные точки [9] [10] [1]
Лазерная терапия [1]
Поверхностное сухое иглоукалывание наиболее эффективно в сочетании с растяжкой позвоночника [2]
Физиотерапия
Боль, возникающая при миофасциальном болевом синдроме, называется отраженной болью. Итак, это терапия для лечения отраженной боли, которая вызывает миофасциальный болевой синдром.
Сухая игла [9] [10] [1] [3]
Массаж [9] [1]
Применение тепла или льда [9]
Чрескожная электрическая стимуляция нервов [9] [10] [1]
Техника распыления и растяжения этилхлорида [9] [10] [1]
Ультразвук [9] [1]
Упражнения [9] [1]
Использованная литература
1.Arendt-Nielsen L, Svensson P (2001). "Referred muscle pain: basic and clinical findings". Clin J Pain 17 (1): 11–9.
2. Ari B.Y., Low Back Pain with Referred Pain, http://www.spine-health.com/conditions/lower-back-pain/low-back-pain-referred-pain 15-04-2012.
3. B. van Cranenburgh. SCHEMA’S FYSIOLOGIE, Elsevier/De Tijdstroom, Maarssen, 1997, 53;65;70.
4. Cummings B., Human Physiology, Silverthorn, Pearson, 5the edition, p. 348.
5. Da silva J.A. et al, Wool, Rheumatology in Practice, p. 12.5 (level of evidence 5)
Mehta N. and George E. , Head, Face, and Neck Pain Science, Evaluation, and Management ; p. 534.
6. Graven-Nielsen T. et al, Stimulus-response functions in areas with experimentally induced referred muscle pain- a psychophysical study, Brain Res, 1997, 744,p. 121-8.
7. Graven-Nielsen T. et al, Quantification of local and referred muscle pain in humans after sequential i.m. injections of hypertonic saline, Pain 1997,69, p. 111-7.
8. Pedersen-Bjergaard U. et al., Algesia and local responses induced by neurokinin A and substance P in human skin and temporal muscle, Peptides, 1989, 10, p.1147-52.
9. Jensen K. et al, Pain and tenderness in human temporal muscle induced by bradykinin and 5 hydroxytryptamine, Peptides, 1990 , 11, p. 1127-32.
Обзор подготовлен Юртаев А.И